NCデータベースの統合解析によるCHIP判別アルゴリズムの構築
研究概要
私たちの体の中では、血液をつくる「造血幹細胞(ぞうけつかんさいぼう)」が毎日働き続けています。しかし年齢を重ねると、これらの細胞の中に少しずつ遺伝子の変化が起こり、特定の細胞だけが増えやすくなることがあります。これを「クローン性造血」と呼び、病気ではない人にもみられます。特に高齢になるほど増える傾向があります。この状態そのものは症状を引き起こすわけではありませんが、心臓病、脳卒中、糖尿病、肺の病気など、さまざまな病気の発症リスクが高くなることがわかってきました。つまり、病気になる"予兆"としてとらえることができる可能性があります。
一方で、最近普及してきたがんの遺伝子検査では、このクローン性造血による変化が、がん細胞の変化と混ざってしまうことがあります。すると、本当はがんとは関係ない変化なのに、がんのものだと判断されてしまうことがあり、検査の結果を正しく読むことが難しくなります。さらに、先天的な遺伝子の変化(生まれつきの体質)とも区別しなければなりません。つまり「がん由来か」「年齢による変化か」「体質によるものか」を見分けることが、とても重要になってきています。
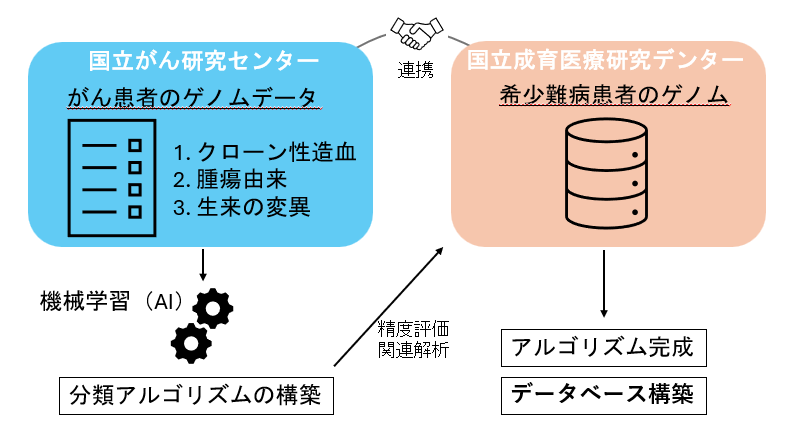
本研究では、その区別を高い精度で行えるようにすることを目指しています。具体的には、多くの患者さんから得られた遺伝子データを活用し、機械学習(AIの一種)を使って、三種類の変化――①がん由来の変化、②クローン性造血による変化、③生まれつきの体質による変化――を見分けられるアルゴリズム(判別方法)をつくります。また、それらをまとめたデータベースも構築します。これにより、通常の検査でも、より正確に遺伝子変化の意味を読み取れるようになることが期待されます。
最終的には、がんや希少な病気との関係も明らかにし、より適切な診断や治療方針の決定につなげていくことが目標です。遺伝子検査が広く使われる時代に向けて、「病気の芽」を正しく捉えるための基盤を築く研究です。
研究のイメージ図
期待される効果
本研究が進むことで、日本人に特有のCHIP(クローン性造血による遺伝子変化)を正確にまとめたデータベースが完成します。これができれば、がんの遺伝子検査で見つかった変化が「がんによるものなのか」「加齢などによるCHIPなのか」をより簡単に判断できるようになります。その結果、患者さんにとってより適切な治療方法を選ぶ助けになることが期待されます。本研究が進むことで、日本人に特有のCHIP(クローン性造血による遺伝子変化)を正確にまとめたデータベースが完成します。これができれば、がんの遺伝子検査で見つかった変化が「がんによるものなのか」「加齢などによるCHIPなのか」をより簡単に判断できるようになります。その結果、患者さんにとってより適切な治療方法を選ぶ助けになることが期待されます。
さらに、CHIPとさまざまな病気との関係を調べることで、病気のリスク因子としてのCHIPを統計的に明らかにできます。これまで、遺伝子の検査結果は「どんな配列か」という点に注目されてきましたが、今後は「CHIPがあるかどうか」という新しい視点を加えることで、ゲノム解析の価値をさらに高めることができます。
主任研究者
池 成基(国立がんセンター東病院 血液腫瘍科 医師)
本研究は、任意の遺伝子変異の由来、特にクローン性造血かどうかを判別するための基盤データをつくることが目的です。がん患者さんにおいては、がんゲノム検査の結果をより正確に解釈できるようになるメリットがあります。もし将来的に健常者のゲノムを調べることができるようになれば、クローン性造血の有無を調べることで生活習慣病や血液腫瘍などの発症リスクを見積もることもできるでしょう。みなさんの健康に役立てるよう、本研究をぜひ成功させたいと思います。

分担研究者
【国立成育医療研究センター】
生命情報学 研究員
青砥 早希